Traduit par le blog http://versouvaton.blogspot.fr
Les dernières données sur la mortalité toutes causes confondues par semaine ne montrent pas une charge hivernale de mortalité statistiquement plus importante que pour les hivers précédents. Il n’y a pas eu de peste. Cependant, un « pic COVID » étroit est présent dans les données, pour plusieurs juridictions en Europe et aux États-Unis.
Ce « pic COVID » de mortalité, toutes causes confondues, présente des caractéristiques uniques :
- Sa netteté, avec une largeur à mi-hauteur maximale de seulement 4 semaines environ ;
- Son retard dans le cycle de la saison infectieuse, avec une augmentation subite après la semaine 11 de 2020, ce qui est sans précédent pour tout pic aigu ;
- La synchronisation du début de sa poussée, sur tous les continents, immédiatement après la déclaration de la pandémie par l’OMS ; et
- Son absence ou sa présence d’un état à l’autre des États-Unis pour la même écologie virale sur le même territoire, étant corrélée aux événements des maisons de retraite et aux actions du gouvernement plutôt qu’à un quelconque discernement de la souche virale connue.
Ces caractéristiques du « pic COVID », ainsi qu’un examen de l’histoire épidémiologique et des connaissances pertinentes sur les maladies respiratoires virales, m’amènent à postuler que le « pic COVID » résulte d’un homicide de masse accéléré de personnes immunovulnérables et de personnes rendues plus immunovulnérables par des actions gouvernementales et institutionnelles, plutôt que d’être la signature épidémiologique d’un nouveau virus, quel que soit le degré de nouveauté du virus du point de vue de la spéciation virale.
Les données sur les causes de décès sont intrinsèquement peu fiables
L’attribution de la cause de la mort, avec les maladies infectieuses et la comorbidité, est non seulement techniquement difficile (par exemple, Simonsen et al., 1997 ; Marti-Soler et al., 2014) mais aussi contaminée par les préjugés des médecins, la politique et les médias.
Cela est connu depuis que l’épidémiologie moderne a été pratiquée pour la première fois. Voici Langmuir (1976) qui cite le célèbre pionnier William Farr, à propos de l’épidémie de grippe de 1847 :
Farr utilise cette épidémie pour réprimander légèrement les médecins sur leurs vues étroites en soulignant que de fortes augmentations ont été observées non seulement avec la grippe elle-même, mais aussi la bronchite, la pneumonie et l’asthme et de nombreuses autres causes non respiratoires, déclare-t-il : … il existe une forte disposition chez certains praticiens anglais non seulement à localiser la maladie, mais aussi à ne voir que la maladie locale. Par conséquent, bien qu’il soit certain que la mortalité élevée enregistrée soit le résultat immédiat de l’épidémie de grippe, les décès évoqués pour cette cause ne sont que de 1 157.
Et, ce biais est généralement reconnu par les principaux épidémiologistes (Lui et Kendal, 1987) :
… la décision de classer les décès en « pneumonie et grippe » est subjective et potentiellement incohérente. D’une part, l’effet de la grippe ou de la pneumonie liée à la grippe peut être sous-estimé car les maladies chroniques sous-jacentes, en particulier chez les personnes âgées, sont généralement mentionnées comme cause de décès sur le certificat de décès. D’autre part, après que l’activité grippale a été publiquement déclarée, il peut y avoir une tendance accrue à classer les décès comme étant dus à « la pneumonie et la grippe », ce qui amplifie le taux d’augmentation des décès liés aux 2 ou, lorsqu’une baisse de l’activité grippale est déclarée, il peut en résulter un biais vers la diminution de la classification des décès liés à « la pneumonie et la grippe ». Aucune enquête n’a été réalisée pour évaluer ces possibilités.
On peut raisonnablement s’attendre à ce que dans le monde actuel des médias sociaux, avec une « pandémie » déclarée par l’Organisation mondiale de la santé (OMS), ce biais ne soit que plus important par rapport à sa présence lors d’épidémies passées de maladies respiratoires virales.
Par exemple, il est difficile d’interpréter la synchronicité de la déclaration du COVID-19 par l’OMS comme une pandémie et le début de l’augmentation observée des cas et des décès de COVID-19 comme étant le produit d’une coïncidence ou de la capacité de prévision extraordinaire du système mondial de surveillance de la santé :
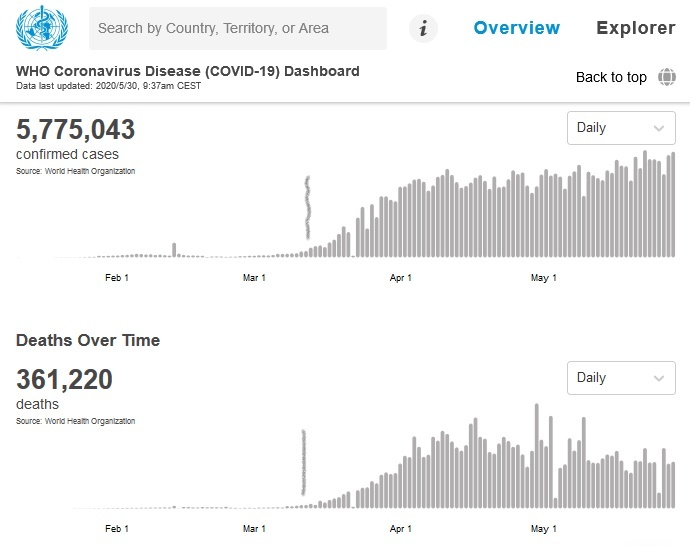
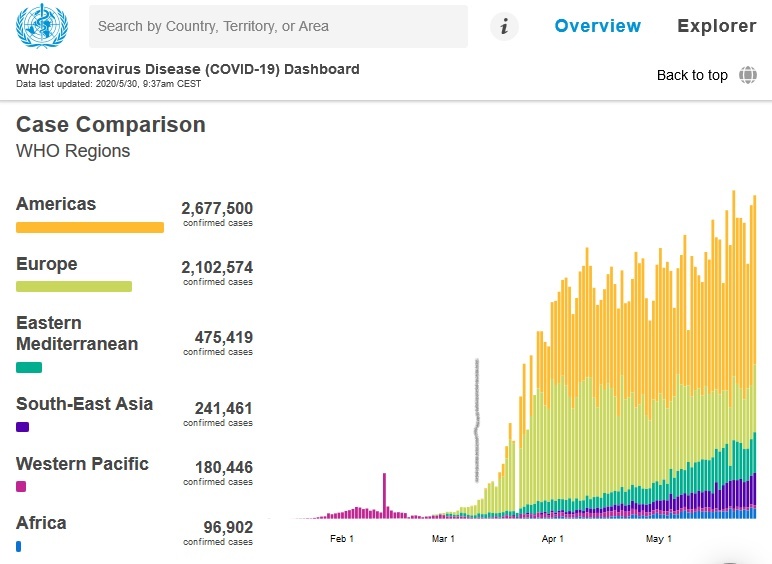
Au contraire, à la lumière des épidémies passées, il est plus probable que ce remarquable phénomène de synchronicité résulte d’attributions biaisées, dans le contexte souple de l’utilisation de tests de laboratoire fabriqués en urgence et non validés, d’évaluations cliniques d’un ensemble générique de symptômes et d’une attribution incertaine de la cause du décès dans des circonstances de comorbidité complexes.
C’est pourquoi les études épidémiologiques rigoureuses s’appuient plutôt sur des données de mortalité toutes causes confondues, qui ne peuvent être modifiées par un biais d’observation ou de déclaration (comme l’indiquent Simonsen et al., 1997 ; et voir Marti-Soler et al., 2014). Un décès est un décès définitif.
La mortalité dans la charge hivernale d’une année sur l’autre dans les pays des latitudes moyennes est très régulière
La mortalité humaine moderne dans les régions à climat tempéré des latitudes moyennes est fortement saisonnière. Les graphiques du nombre de décès toutes causes confondues par unité de temps (mois, semaine, jour), dans des régions données, présentent un schéma annuel, avec une amplitude de pic à creux de 10 à 30 % de la valeur de base du creux, en grande partie indépendamment des agents pathogènes spécifiques qui peuplent les saisons spécifiques. Une forte mortalité se produit en hiver, et est donc inversée dans les hémisphères nord et sud (par exemple, Marti-Soler et al., 2014).
Pour les États-Unis, le phénomène est bien illustré dans cette figure de Simonsen et al. (1997) :
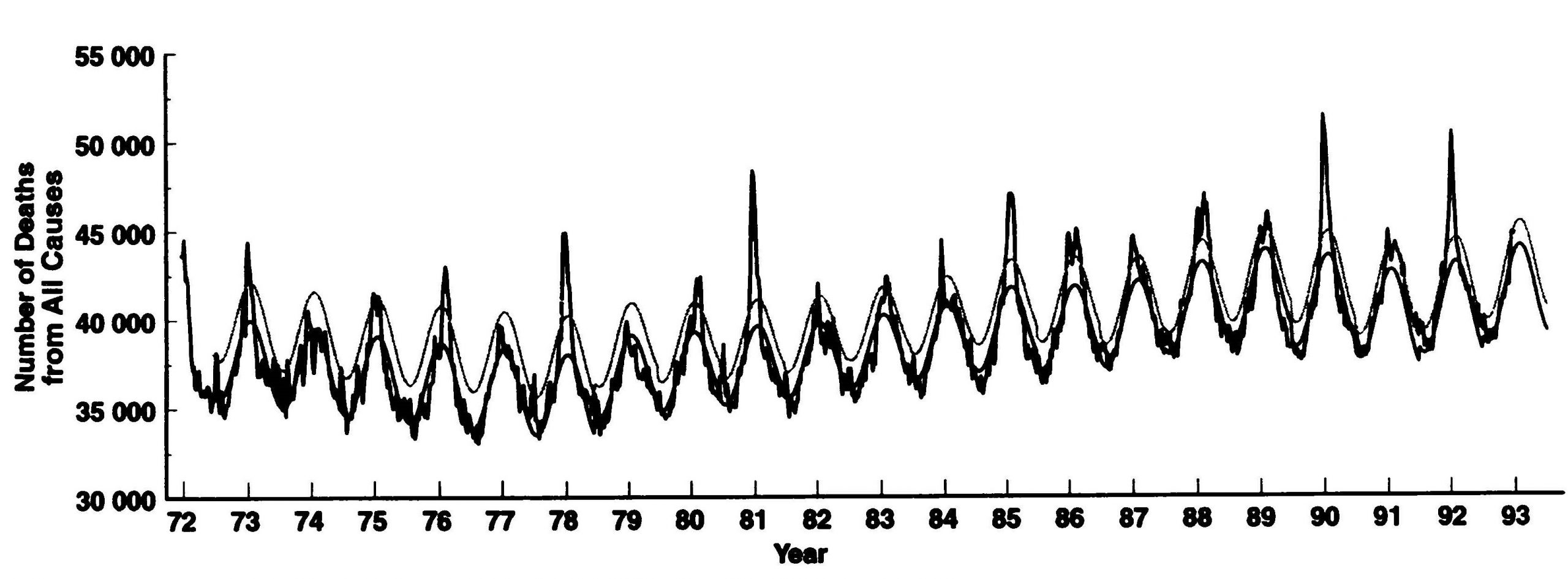
Dans un tel graphique, la zone située sous un pic, par rapport à son niveau de référence minimal, est le nombre total de décès annuels l’hiver, au-dessus du niveau de référence minimal. Le nombre « excédentaire » de décès annuel ainsi calculé, ici (dans la période 1972-1993), est toujours d’environ 8 à 11 % du total des décès annuels au niveau de référence minimal, ainsi que d’environ 8 à 11 % de la mortalité annuelle toutes causes confondues.
Cette « surmortalité » régulière et saisonnière, ou charge hivernale, a été un défi épidémiologique à comprendre, même si, à commencer par Farr, de nombreux épidémiologistes l’ont initialement attribuée presque entièrement aux maladies respiratoires virales de type grippe saisonnière.
Néanmoins, l’angoissante difficulté à comprendre la ou les causes de ce schéma remarquablement régulier et global (les deux hémisphères, mais inversé) persiste, comme l’illustrent les propos de Marti-Soler et al. (2014) (références omises) :
Étant donné que la mortalité due au cancer ne présente pratiquement pas de schéma de saisonnalité, la saisonnalité de la mortalité globale est principalement due à la saisonnalité de la mortalité due aux MCV [maladies cardiovasculaires] et à la mortalité non due aux MCV et non due au cancer. Pour ces conditions, et en particulier pour les MCV, l’exposition au froid est une explication plausible de la saisonnalité observée, étant donné la relation entre le climat froid et la latitude. Plusieurs études longitudinales ont démontré qu’une baisse de la température extérieure était associée à une augmentation de la mortalité toutes causes confondues. Cependant, d’autres facteurs dépendant de la latitude, tels que les habitudes alimentaires, l’exposition au soleil (taux de vitamine D) et les agents parasitaires et infectieux humains pourraient également jouer un rôle. L’ampleur du schéma saisonnier de la mortalité due aux MCV était plus élevée que celle de la mortalité toutes causes confondues. Le caractère saisonnier de la mortalité due aux MCV pourrait être dû en partie à la saisonnalité conjointe de plusieurs facteurs de risque connus de MCV, comme décrit précédemment. De même, les facteurs liés au mode de vie, tels que l’alimentation et l’activité physique, ont également tendance à différer pendant les mois d’été et d’hiver. De plus, l’exposition au froid augmente la dépense énergétique, la vasoconstriction périphérique et la post-charge cardiaque, ce qui peut déclencher une ischémie myocardique et un accident vasculaire cérébral. Enfin, l’infection grippale à tendance hivernale peut également être un déclencheur de décès dus à des maladies cardio-vasculaires en exacerbant les conditions de ces maladies ou en raison de complications secondaires. C’est probablement le cas de la concentration des polluants atmosphériques.
La saisonnalité de la mortalité non liée aux MCV et non liée au cancer peut être liée au fait que les maladies pulmonaires obstructives chroniques et la pneumonie sont des maladies fréquentes dans cette catégorie et que ces maladies sont exacerbées par la grippe, d’autres infections de type grippal et les concentrations de polluants atmosphériques, qui sont toutes plus fréquentes en hiver. Quelques autres maladies de la catégorie des maladies non dues aux MCV et non dues au cancer présentent également un schéma saisonnier, par exemple la dépression, le suicide et les hémorragies variqueuses de l’œsophage.
Pourquoi la mortalité dans sa charge hivernale est-elle si régulière et persistante ?
Même la saisonnalité de la partie « pneumonie et grippe » (P&G) qui représente une grande partie de ce que Marti-Soler et al. quantifient comme « mortalité non due aux MCV et non due au cancer » n’a été comprise qu’il y a dix ans. Jusqu’à récemment, on se demandait si le schéma annuel des P&G était principalement dû aux changements saisonniers de la virulence des agents pathogènes ou aux changements saisonniers de la sensibilité de l’hôte (par exemple, l’air sec provoquant une irritation des tissus, ou la diminution de la lumière du jour entraînant une carence en vitamines ou un stress hormonal). Voir, par exemple, Dowell (2001). Dans un sens, la réponse est « ni l’un ni l’autre ».
Dans une étude qui fait date, Shaman et al. (2010) ont montré que le schéma saisonnier de surmortalité des maladies respiratoires (P&G) peut être expliqué quantitativement sur la seule base de l’humidité absolue, et son impact direct sur la transmission des pathogènes aéroportés.
Lowen et ses collègues (2007) ont démontré que le phénomène de contagiosité des virus aériens dépend de l’humidité dans la transmission réelle de maladies entre cobayes, et ont examiné les mécanismes sous-jacents potentiels de l’effet de contrôle mesuré de l’humidité.
Le mécanisme sous-jacent est que les particules ou les gouttelettes de la taille d’un aérosol chargées d’agents pathogènes sont neutralisées à une demi-vie et diminuent de manière linéaire et significative avec l’augmentation de l’humidité absolue ambiante. Ce mécanisme est basé sur les travaux fondateurs de Harper (1961). Harper a montré expérimentalement que les gouttelettes porteuses de virus et d’agents pathogènes étaient inactivées dans des délais de plus en plus courts, à mesure que l’humidité absolue ambiante augmentait.
Harper a soutenu que les virus eux-mêmes étaient rendus inopérants par l’humidité (« décomposition viable »), mais il a admis que l’effet pouvait être dû à l’élimination physique ou à la sédimentation gravitationnelle des gouttelettes (« perte physique ») : « Les viabilités des aérosols rapportées dans cet article sont basées sur le rapport entre la charge virale et la numération radioactive dans les échantillons de suspension et de nuages, et peuvent être critiquées au motif que les matériaux de test et de traçage n’étaient pas physiquement identiques ».
Cette dernière (« perte physique ») me semble plus plausible, puisque l’humidité absolue aurait pour effet physique universel de provoquer la croissance par condensation et la sédimentation gravitationnelle des particules/gouttelettes (et, inversement, la perte par évaporation et aérosolisation), et que tous les agents pathogènes viraux testés ont essentiellement la même « décomposition » due à l’humidité. En outre, il est difficile de comprendre comment un virion (de n’importe quel type de virus) dans une gouttelette serait attaqué ou endommagé au niveau moléculaire ou structurel par une augmentation de l’humidité ambiante. Un « virion » est la forme complète et infectieuse d’un virus en dehors d’une cellule hôte, avec un noyau d’ARN ou d’ADN et une capside. Aucun mécanisme moléculaire réel ou autre de la « décomposition viable » d’un virion par l’humidité à l’intérieur d’une gouttelette, postulée par Harper (1961), n’a, à ce jour, été expliqué ou étudié, alors que la sédimentation gravitationnelle (« perte physique ») est bien comprise.
Quoi qu’il en soit, l’explication et le modèle de Shaman et al. (2010) ne dépendent pas du mécanisme particulier de la décomposition des virions en aérosol/gouttelettes induite par l’humidité absolue. Le modèle d’épidémiologie virale régionale saisonnière quantitativement démontré par Shaman est valable pour l’un ou l’autre mécanisme (ou combinaison de mécanismes), que ce soit la « décomposition viable » ou la « perte physique ».
La percée réalisée par Shaman et al. n’est pas seulement un sujet académique. Elle a de profondes implications en matière de politique de santé, qui ont été entièrement ignorées ou négligées dans la pandémie actuelle de coronavirus :
- Cela signifie que le caractère saisonnier de la mortalité des P&G est directement lié à la contagiosité des maladies respiratoires virales contrôlée par l’humidité absolue.
Si mon point de vue sur le mécanisme est correct (c’est-à-dire « perte physique » plutôt que « décomposition viable »), alors :
- Cela implique en outre que le vecteur de transmission doit être de petites particules d’aérosol en suspension dans l’air, respirées profondément dans les poumons, à l’intérieur ; et non des voies de transmission hypothétiques comme un contact réel avec un fluide ou un fomite, et non de grosses gouttelettes et de la salive (qui sont rapidement éliminées de l’air par gravitation, ou capturées dans la bouche et le système digestif).
- Et cela signifie que la distanciation sociale, les masques et le lavage des mains peuvent avoir peu d’effet sur la propagation réelle de l’épidémie pendant la saison hivernale (voir : Rancourt, 2020).
En ce qui concerne la modélisation épidémiologique, les travaux de Shaman impliquent que, plutôt que d’être un nombre fixe (dépendant uniquement de la structure spatio-temporelle des interactions sociales dans une population complètement et variablement sensible, et de la souche virale), le nombre de reproduction de base de l’épidémie (R0) dépend principalement de l’humidité absolue ambiante. Pour une définition du R0, voir HealthKnowlege-UK (2020) : R0 est « le nombre moyen d’infections secondaires produites par un cas typique d’infection dans une population où tout le monde est sensible ».
Shaman et al. ont montré que le R0 doit être compris comme variant selon les saisons entre des valeurs d’été humide légèrement supérieures à « 1 » et des valeurs d’hiver sec généralement aussi élevées que « 4 » (voir par exemple leur tableau 2). En d’autres termes, les maladies respiratoires virales infectieuses saisonnières qui sévissent chaque année dans les régions à climat tempéré passent d’une contagion intrinsèquement légère à une contagion virulente, simplement en raison du mode de transmission biophysique contrôlé par l’humidité absolue de l’air, largement indépendamment de toute autre considération.
En outre, il a été démontré que les concentrations de virus dans l’air intérieur (dans les garderies, les centres de santé et à bord des avions) existent principalement sous forme de particules d’aérosol de diamètre inférieur à 2,5 μm, comme le montrent les travaux de Yang et al. (2011) :
La moitié des 16 échantillons étaient positifs, et leurs concentrations totales en virus variaient de 5 800 à 37 000 copies du génome m-3. En moyenne, 64 % des copies du génome viral étaient associées à des particules fines de diamètre inférieur à 2,5 μm, qui peuvent rester en suspension pendant des heures. La modélisation des concentrations de virus à l’intérieur a suggéré une force de source de 1,6 ± 1,2 × 105 copies du génome m-3 dans l’air h-1 et un flux de dépôt sur les surfaces de 13 ± 7 copies du génome m-2 h-1 par mouvement brownien. Sur une heure, la dose d’inhalation a été estimée à 30 ± 18 dose infectieuse médiane en culture tissulaire (TCID50), suffisante pour induire l’infection. Ces résultats apportent un soutien quantitatif à l’idée que la voie aérosol pourrait être un mode important de transmission de la grippe.
Note de l'auteur "h-1" signifie "par heure". "m-3" signifie "par mètre cube" et indique un volume. "m-2" signifie "par mètre carré" et indique une surface. "m-3 h-1" signifie donc "par mètre cube par heure".
Ces petites particules (inférieures à 2,5 μm) font partie de la fluidité de l’air, ne sont pas soumises à la sédimentation gravitationnelle et peuvent donc être respirées profondément dans les poumons.
La question suivante est la suivante : combien de particules chargées d’agents pathogènes de ce type sont nécessaires pour provoquer une infection chez une personne ayant une capacité moyenne de réponse immunitaire ?
Yezli et Otter (2011), dans leur examen de la dose infectieuse minimale (DIM), soulignent les caractéristiques pertinentes :
- la plupart des virus respiratoires sont aussi infectieux chez l’homme que dans les cultures de tissus ayant une sensibilité optimale en laboratoire
- la MID à 50 % de probabilité (« TCID50 ») se situe, de manière variable, entre 100 et 1000 virions
- il y a généralement 103-107 virions par gouttelette de grippe aérosol de 1 μm à 10 μm de diamètre
- la MID à 50 % de probabilité s’insère facilement dans une seule gouttelette aérosolisée
Pour en savoir plus :
- Haas (1993) fournit une description classique de l’évaluation dose-réponse.
- Zwart et al. (2009) ont fourni la première preuve en laboratoire, dans un système virus-insecte, que l’action d’un seul virion peut être suffisante pour provoquer une maladie.
- Baccam et al. (2006) ont calculé, à partir de données empiriques, qu’avec la grippe A chez l’homme, « nous estimons qu’après un délai de ~6 h, les cellules infectées commencent à produire le virus de la grippe et continuent à le faire pendant ~5 h. La durée de vie moyenne des cellules infectées est de ~11 h, et la demi-vie du virus infectieux libre est de ~3 h. Nous avons calculé le nombre de reproduction de base [dans le corps], R0, qui indique qu’une seule cellule infectée peut produire ~22 nouvelles infections productives ».
- Brooke et al. (2013) ont montré que, contrairement aux hypothèses de modélisation précédentes, bien que toutes les cellules infectées par le virus de la grippe A dans le corps humain ne produisent pas une progéniture infectieuse (virions), néanmoins, 90 % des cellules infectées sont significativement affectées.
L’examen ci-dessus signifie que toutes les maladies respiratoires virales qui frappent chaque année les populations des régions tempérées sont extrêmement contagieuses pour deux raisons : (1) elles sont transmises par de petites particules d’aérosol qui font partie de l’air fluide et remplissent pratiquement tous les espaces d’air clos occupés par les humains, et (2) une seule de ces particules d’aérosol porte la dose infectieuse minimale (DIM) suffisante pour provoquer une infection chez une personne, si elle est inhalée dans les poumons, où l’infection est initiée.
C’est pourquoi le schéma de mortalité toutes causes confondues est si solidement stable et réparti dans le monde entier, si l’on admet que la majorité de la charge est induite par des maladies respiratoires virales, tout en étant relativement insensible à l’écologie virale saisonnière particulière pour cette classe opérationnelle de virus. Cela explique également pourquoi le schéma est inversé entre l’hémisphère nord et l’hémisphère sud, indépendamment des voyages aériens touristiques et d’affaires et ainsi de suite.
Les virologues et les généticiens voient les souches, les mutations et les espèces virales (Alimpiev, 2019), comme un homme avec un marteau voit des clous. De même, il existe des récompenses professionnelles pour l’identification de nouveaux agents pathogènes viraux et la description de nouvelles maladies. Pour ces raisons, les scientifiques n’ont pas vu la forêt mais les arbres.
Mais les données montrent qu’il existe un schéma persistant et régulier de mortalité dans la charge hivernale, indépendamment des détails, et que la répartition du nombre de décès excédentaires d’une année sur l’autre est bien limitée (environ 8 à 11 % de la mortalité annuelle totale, aux États-Unis, de 1972 à 1993). Malgré tout ce qu’on dit sur les épidémies, les pandémies et les nouveaux virus, le schéma est résolument constant.
Une anomalie digne de panique, et d’une ingénierie socio-économique mondiale nocives, devrait consister en une mortalité de charge hivernale annuelle d’origine naturelle statistiquement supérieure à la norme. Cela ne s’est pas produit depuis l’unique pandémie de grippe de 1918 (Hsieh et al., 2006).
Les trois épidémies récentes qualifiées de pandémies, à savoir la pandémie H2N2 de 1957, la pandémie H3N2 de 1968 et la pandémie H1N1 de 2009, n’ont pas été plus virulentes (en termes de mortalité annuelle dans la charge hivernale) que les épidémies saisonnières régulières (Viboud et al., 2010 ; Viboud et al., 2006 ; Viboud et al., 2005). En fait, l’épidémie de 1951 a été jugée plus meurtrière, sur la base des données de P&G, en Angleterre, au Pays de Galles et au Canada, que les pandémies de 1957 et 1968 (Viboud et al., 2006).
Un modèle simple de virulence de facto des maladies respiratoires virales
Face à la persistance et à la régularité de la charge hivernale de la mortalité, on est tenté de proposer que les propriétés spécifiques (structurelles, moléculaires et de liaison) de l’agent pathogène viral d’une maladie respiratoire particulière ne sont pas aussi déterminantes pour la mortalité que les virologues le suggèrent. Au contraire, il est possible que la mortalité, dans une population donnée exposée à ces agents pathogènes viraux hautement contagieux qui envahissent les poumons, soit principalement contrôlée par la répartition de la population en terme de capacité et de préparation du système immunitaire.
Une charge virale pénètre dans les poumons. Une fois que l’antigène viral est reconnu, une réponse immunitaire se met en place1. Une « guerre » dynamique s’ensuit entre le virus qui se reproduit et se propage en infectant les cellules de la paroi des poumons, et le système immunitaire qui fait tout ce qu’il peut pour identifier, localiser et détruire les cellules infectées avant que lesdites cellules infectées ne puissent être productives du virus.
La réponse immunitaire est extraordinairement exigeante pour les ressources énergétiques métaboliques de l’organisme (c’est pourquoi il faut « nourrir un rhume », « se reposer » et « rester au chaud »). La demande en énergie métabolique est prioritaire et peut concurrencer les demandes des fonctions corporelles essentielles et les réponses immunitaires à d’autres agents pathogènes. C’est pourquoi les personnes souffrant de maladies « liées à l’âge » et de comorbidité sont particulièrement exposées : leur taux d’apport d’énergie métabolique au système immunitaire est limité par leurs co-conditions, et la demande n’est pas satisfaite à un rythme suffisamment élevé pour gagner la « guerre ». Voir : Straub (2017) ; Bajgar et al. (2015).
Dans une vue simple de l’infection (que je propose pour illustration), un individu donné, ayant un état de santé donné, ne peut fournir de l’énergie métabolique au système immunitaire que jusqu’à un certain taux maximum de fourniture, pendant la phase cruciale de la « guerre ». C’est ce que l’on appelle le « taux d’apport énergétique pour la réponse immunitaire » : RS. Le RS est exprimé en unités d’énergie par unité de temps, J/s, ou en calories par seconde. Si le RS est suffisant pour « gagner la guerre » et est maintenu suffisamment longtemps, alors l’individu se remet de l’infection et le système immunitaire stocke une mémoire moléculaire de l’antigène viral, ce qui réduit considérablement la demande en énergie pour les futures réponses immunitaires aux attaques du même virus ou d’un virus suffisamment similaire. Si la réponse immunitaire est insuffisante, l’individu succombe au virus et meurt.
Par conséquent, le virus saisonnier peut être caractérisé comme ayant une valeur de RS spécifique au virus, dites RSv, qui est le seuil de RS pour la survie de la personne infectée. Si RS > RSv, alors la personne se rétablit. Si RS < RSv, alors la personne meurt. Plus le RSv est élevé, plus le virus est virulent, et vice versa.
Une population humaine donnée (nationale ou régionale) aura une distribution donnée des valeurs de RS associée aux différents membres de la population.
Mathématiquement, cette distribution peut être représentée comme une densité de probabilité des valeurs de RS. Une valeur de densité de probabilité comporte des unités de nombre de personnes par unité d’intervalle de RS. La surface totale sous la courbe de densité de probabilité est la population, de la nation ou de la région.
La figure 4 illustre trois distributions hypothétiques des valeurs de RS, dans trois populations différentes de taille égale. Ici : « Allemagne/Germany » (ligne bleue continue) correspond à une population occidentale actuelle, qui ne compte pas une population âgée particulièrement nombreuse ; « Italie » (ligne bleue pointillée) correspond à une population occidentale actuelle qui compte une population âgée nombreuse ; et « Stressed » (ligne rouge continue) correspond à une population d’individus soumis à un stress métabolique (ou sanitaire) élevé, comme cela a pu être le cas en Angleterre en 1918.
Un tel stress pour la santé peut être dû à une carence nutritionnelle, à un manque de nutriments essentiels ou de vitamines, à des niveaux élevés d’agents stressants environnementaux, de toxines ou d’agents pathogènes, à une pénurie de logements [ou de la capacité à le chauffer, NdSF](« fuel poverty« ), à des conditions de travail oppressives, à l’oppression de la domination sociale, à l’abus de substances provoquant des lésions organiques, etc. Il existe une vaste littérature sur ces facteurs. Comme point d’ancrage, voir : Sapolsky (2015) ; Sapolsky (2005).
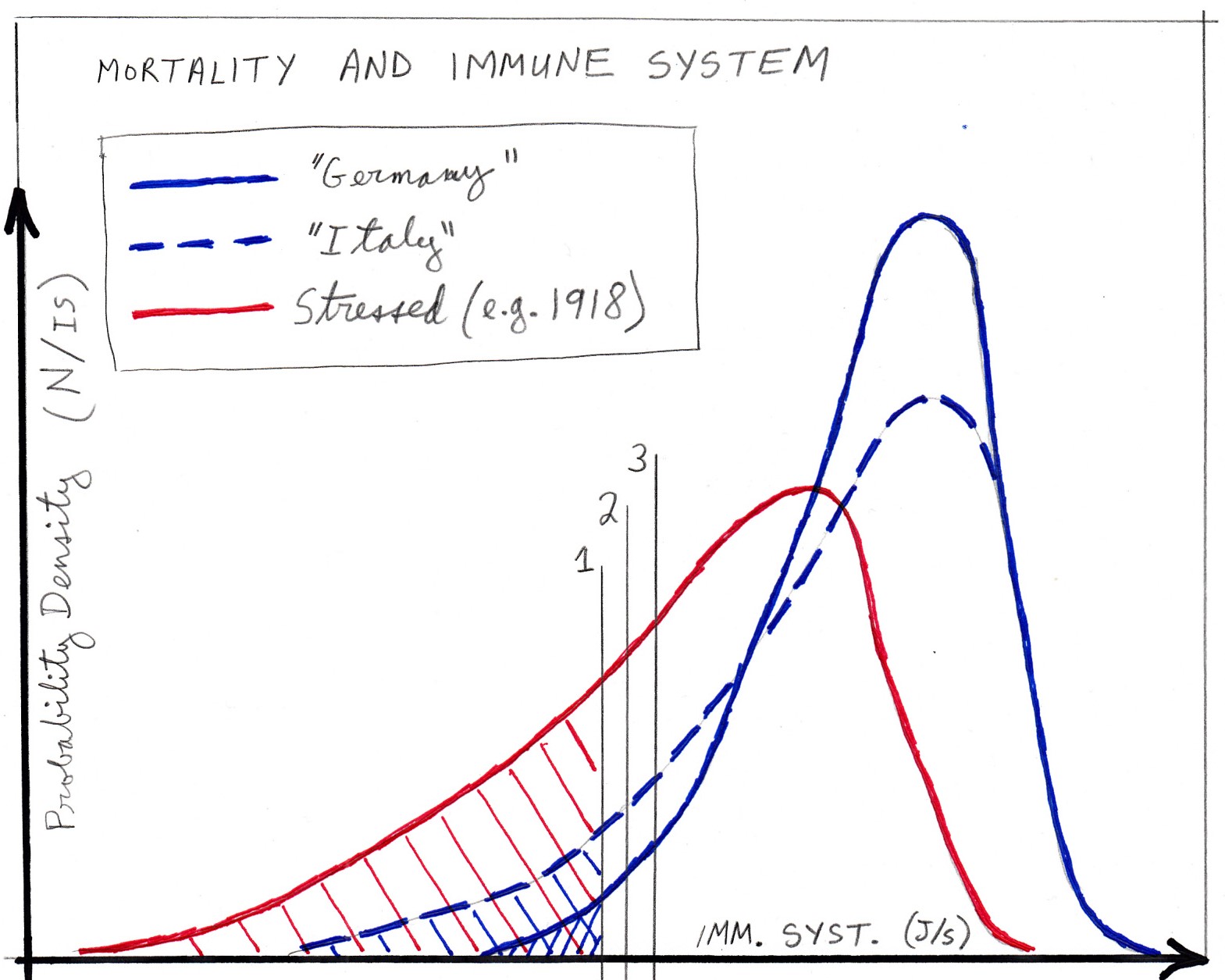
Dans ce modèle, la mortalité comparative entre les populations, pour un agent pathogène viral donné, est donc déterminée par les différents états de santé (distributions des valeurs de RS des individus) des populations infectées comparées.
Cela concerne le cycle complet de l’infection et de la guérison. Il en dit peu sur les taux de mortalité quotidiens et les distributions par âge, qui dépendent de la propagation naturelle ou forcée de l’infection, qui à son tour n’est pas nécessairement uniforme dans le temps et l’espace mais peut plutôt cibler des segments particuliers de la population, comme les personnes confinées dans des institutions.
En outre, la distribution des valeurs de RS pour une population donnée peut changer de manière significative au cours d’une épidémie, si les segments vulnérables sont soumis à des facteurs de stress supplémentaires en matière de santé, par exemple.
Analyse de la mortalité toutes causes confondues de COVID-19 et les modélisations de déconvolutions
À la lumière du contexte et des outils conceptuels ci-dessus, nous pouvons maintenant examiner les données liées au COVID-19, à ce jour. Pour de bonnes raisons (voir ci-dessus), nous ignorons les données relatives aux décès et les modélisations de déconvolutions des décès P&G par rapport à d’autres décès jugés saisonniers pour des raisons non liées aux agents pathogènes viraux saisonniers. Nous nous concentrons sur la mortalité toutes causes confondues, par semaine.
La mortalité toutes causes confondues n’est pas susceptible de biais et est actuellement disponible pour plusieurs juridictions. Nous utilisons les données brutes sans aucune manipulation, et nous ne modifions pas les données pour les « corriger » en fonction des changements de la population totale ou de la structure d’âge d’une population.
Pour les données, nous nous appuyons sur le CDC (USA), les données des instituts nationaux pour l’Angleterre et le Pays de Galles, et les compilations graphiques du centre EuroMOMO. Nous n’utilisons que les dernières semaines qui sont déclarées complètes (« >100% », CDC) ou jugées de qualité suffisante pour être publiées. Malheureusement, certaines juridictions telles que le Canada peuvent être caractérisées comme lentes et réfractaires aux demandes.
La figure 5 montre la mortalité toutes causes confondues par semaine pour l’Angleterre et le Pays de Galles, à partir de 2010. Les baisses soudaines sur une semaine sont des incohérences dans la comptabilité et dans les délais de certification des décès, qui sont comptées dans la ou les semaines suivantes. La ligne verticale rouge indique la date à laquelle l’OMS a déclaré la pandémie.
En déclarant la pandémie, le directeur général de l’OMS, Tedros Adhanom, a notamment déclaré2 :
[…] Dans les jours et les semaines à venir, nous nous attendons à voir le nombre de cas, le nombre de décès et le nombre de pays touchés augmenter encore plus. […] Et nous avons appelé chaque jour les pays à prendre des mesures urgentes et énergiques. Nous avons tiré la sonnette d’alarme haut et fort. […]
Il ne s’agit pas seulement d’une crise de santé publique, mais d’une crise qui touchera tous les secteurs – chaque secteur et chaque individu doit donc être impliqué dans la lutte.
J’ai dit dès le début que les pays doivent adopter une approche pan-gouvernementale et sociétale, construite autour d’une stratégie globale pour prévenir les infections, sauver des vies et minimiser l’impact. […]
Je rappelle à tous les pays que nous vous demandons d’activer et de renforcer vos mécanismes d’intervention d’urgence ; de communiquer avec votre population sur les risques et la manière dont elle peut se protéger – c’est l’affaire de tous ; de trouver, isoler, tester et traiter chaque cas et de retracer chaque contact ; de préparer vos hôpitaux ; [C’est moi qui souligne, NdA].
Les propos d’Adhanom ont soit constitué la prévision de santé publique la plus remarquable jamais faite pour l’Angleterre et le Pays de Galles (et de nombreuses juridictions dans le monde, voir ci-dessous), soit quelque chose d’autre pourrait expliquer le pic de mortalité toutes causes confondues qui a immédiatement suivi sa déclaration.
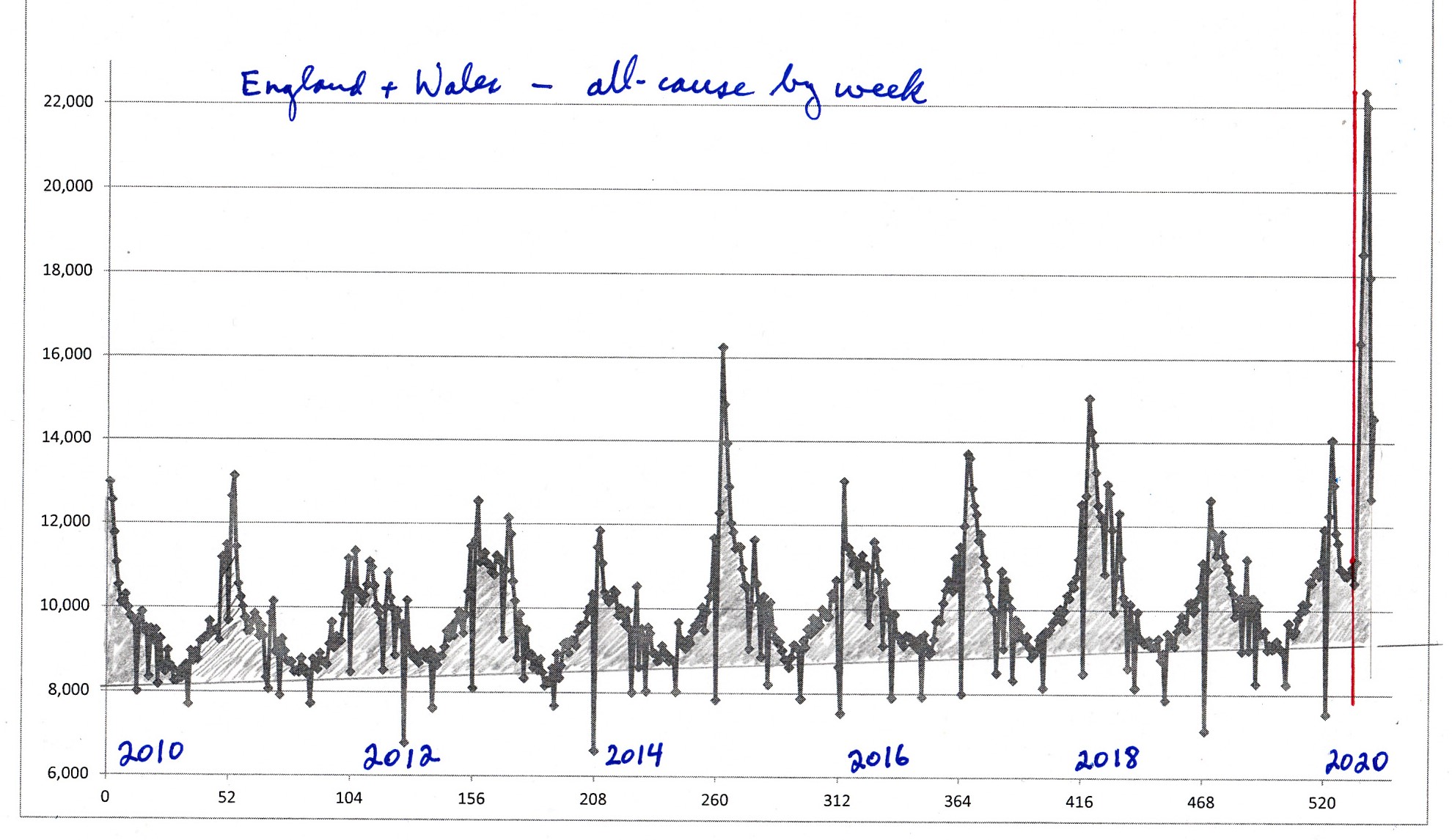
Il est important de noter que le nombre total de décès « excédentaires », toutes causes confondues, la charge hivernale pour la saison se terminant en 2020 (zone au-dessus de la ligne de base de l’été), n’est pas statistiquement plus élevé que pour les années passées, et il reste à voir jusqu’à quel point le creux de l’été 2020 sera bas.
Ce que l’on peut appeler le « pic COVID » est une caractéristique étroite (figure 5). Par rapport à la ligne de base estivale, la largeur totale à mi-hauteur du pic est d’environ 5 semaines. Il se distingue par le fait qu’il se situe à la fin de la saison infectieuse et qu’il s’élève bien au-dessus de la bosse plus large de la charge hivernale.
Ce « pic COVID » est un événement unique dans l’histoire épidémiologique de l’Angleterre et du Pays de Galles. Cette caractéristique unique est-elle due à un agent pathogène viral inhabituellement nouveau, ou à la réponse unique, sans précédent et massive du gouvernement à la déclaration de pandémie de l’OMS ?
Notez qu’un tel « pic COVID » n’implique pas une virulence intrinsèque du virus. Cela signifie seulement que les décès de personnes vulnérables, ou de personnes rendues vulnérables, sont survenus dans un court laps de temps. Par exemple, les personnes qui seraient mortes dans les semaines ou les mois suivants peuvent voir leur décès accéléré par l’intervention humaine, ou celles qui se remettent encore d’une infection virale peuvent être poussées dans des conditions de vie plus précaires et plus stressantes.
Un « pic COVID » analogue s’est produit dans les données du centre EuroMOMO pour l’Europe (figure 6). Là encore, le nombre total de décès excessifs, toutes causes confondues, de la charge hivernale pour la saison se terminant en 2020 (zone au-dessus de la ligne de base estivale) n’est pas statistiquement plus élevé que pour les années passées, et la date de déclaration de la pandémie est indiquée par une ligne rouge verticale.
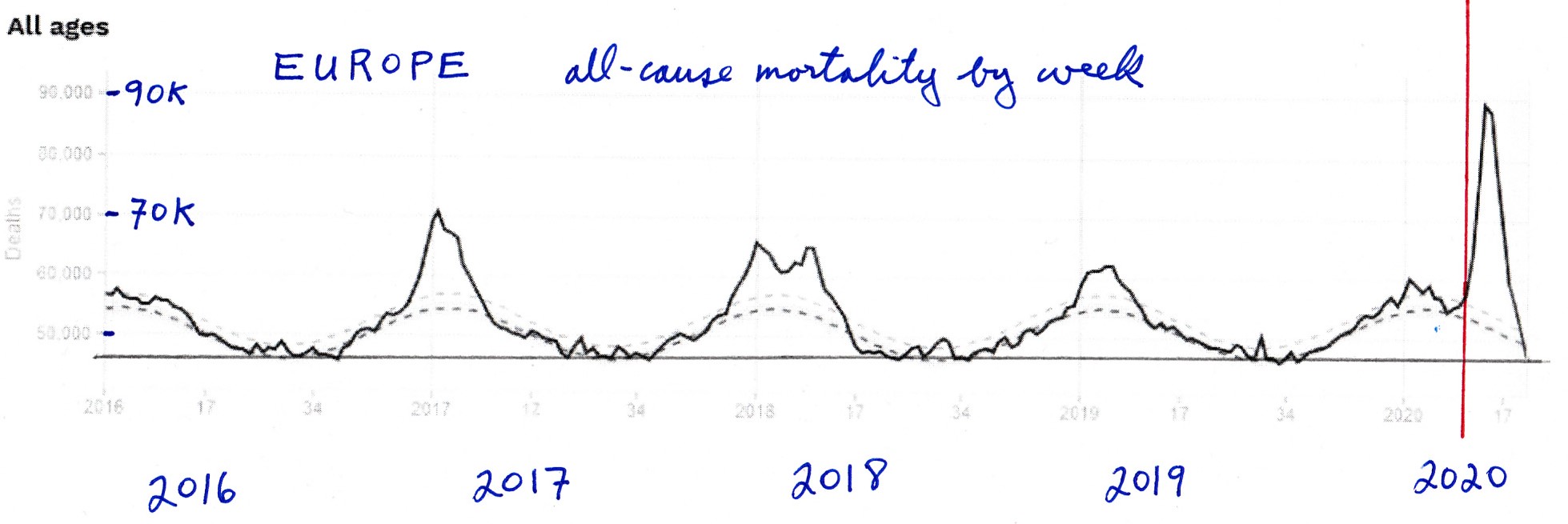
Ce qui ressemblait à une saison 2020 « douce » et concluante s’est transformé en « pic COVID » immédiatement après la déclaration de la pandémie par l’OMS.
Passons maintenant aux États-Unis, où les données actuelles sont facilement accessibles, tant au niveau national qu’au niveau de chaque État, grâce au CDC.
La figure 7 montre la mortalité toutes causes confondues par semaine pour les États-Unis, à partir de 2014. Ici, la base de référence pour l’été est d’environ de 46 000 à 52 000 décès par semaine, qui augmentent avec l’augmentation de la population totale. La ligne verticale rouge indique la date à laquelle l’OMS a déclaré la pandémie de COVID-19.
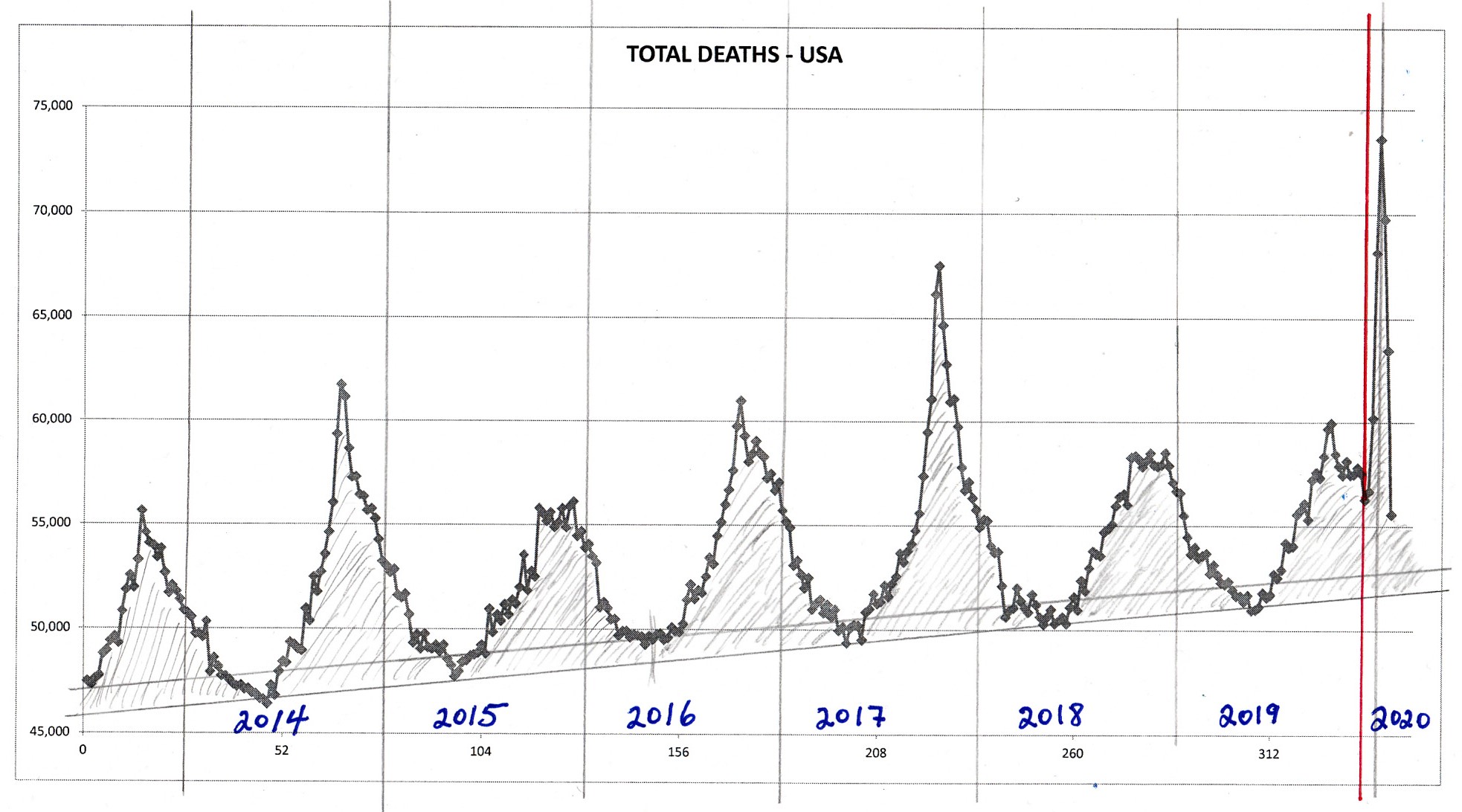
Ici encore, nous constatons que le nombre total de décès toutes causes confondues de la charge hivernale pour la saison se terminant en 2020 (zone au-dessus de la ligne de base estivale) n’est pas statistiquement plus élevé que pour les dernières années. Il n’y a aucune preuve, uniquement en termes de nombre de décès saisonniers, qui suggère un événement catastrophique ou un agent pathogène exceptionnellement virulent. Il n’y a pas eu de « fléau ». La charge hivernale, au cours de ces années, se situe constamment dans une fourchette d’environ 6 à 9 % de la mortalité annuelle totale toutes causes confondues, et les variations d’une année sur l’autre sont typiques des variations historiques.
D’autre part, il existe à nouveau un « pic COVID », qui présente les caractéristiques uniques suivantes :
- Il est remarquablement net ou étroit, sa largeur à mi-hauteur du pic, par rapport à la ligne de base de l’été, n’étant que de 4 semaines environ. En comparaison, les pics importants des saisons infectieuses se terminant en 2015 et 2018 ont une largeur maximale de 14 et 9 semaines, respectivement.
- Il se produit plus tard dans la saison infectieuse que tout autre pic important jamais observé aux États-Unis, et il augmente après la semaine 11 de 2020.
- Sa montée survient immédiatement après la déclaration de la pandémie par l’OMS, en parfaite synchronisation, comme on peut le voir en Europe, en Angleterre et au Pays de Galles, qui sont séparés des États-Unis par un océan.
Le « pic COVID » dans les données américaines provient de « points chauds », comme la ville de New York (NYC). La figure 8 montre la mortalité toutes causes confondues par semaine pour NYC, à partir de 2013. La ligne verticale rouge indique la date à laquelle l’OMS a déclaré la pandémie COVID-19.
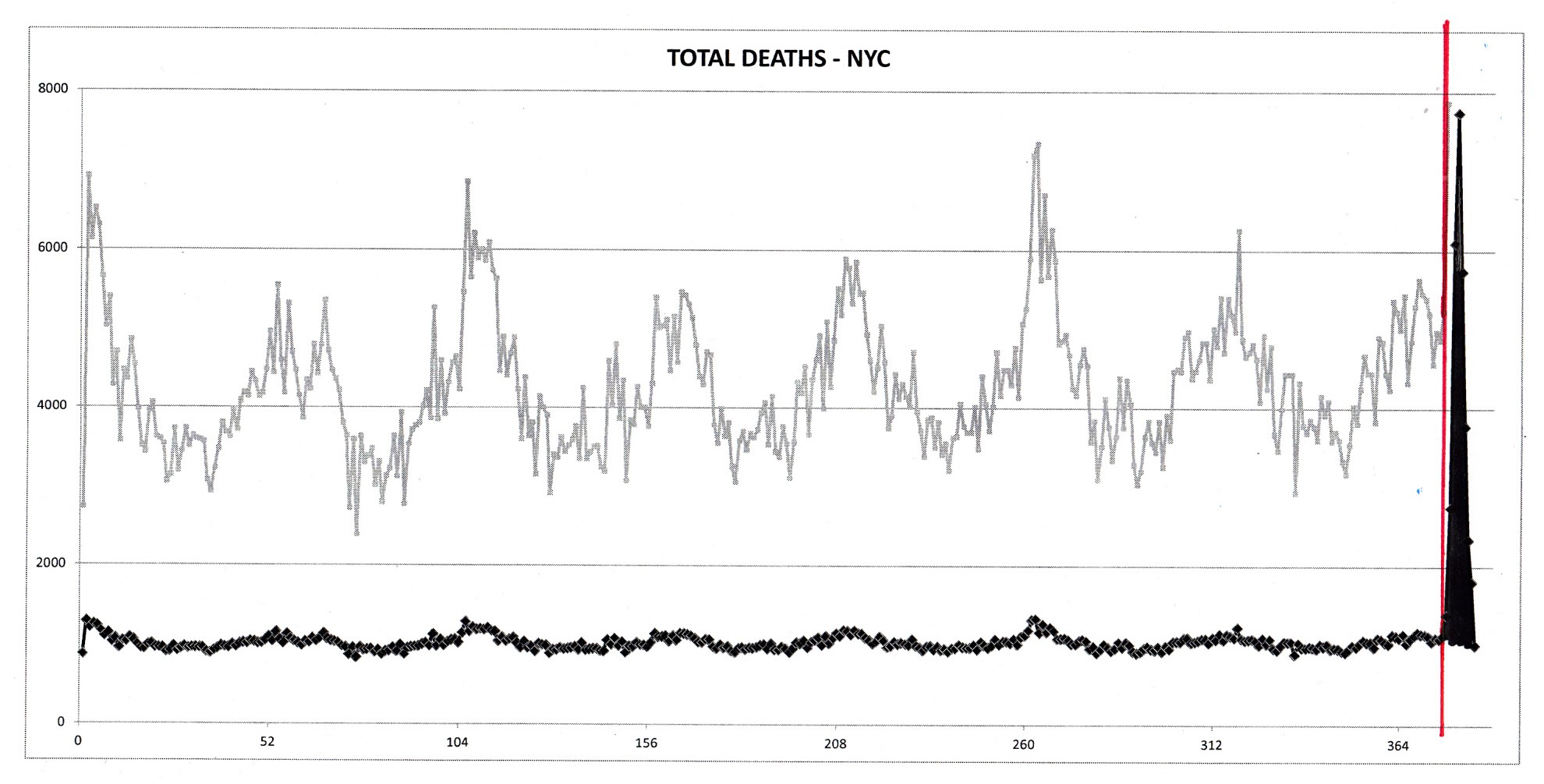
Les données de NYC n’ont aucun sens épidémiologique. Le « pic COVID » ici, à première vue, ne peut pas être interprété comme un processus normal de maladie respiratoire virale dans une population sensible. Des effets locaux, tels que l’importation de patients d’autres juridictions ou de fortes densités de personnes vulnérables institutionnalisées ou hébergées, doivent au moins être en jeu.
Ce qui est également frappant, c’est que certains des États américains les plus peuplés, qui comptent un grand nombre de cas mesurés et signalés, et un grand nombre de personnes présentant les anticorps, ne présentent pas de « pic de COVID ». (Les anticorps caractéristiques sont produits et présents dans le corps des individus qui ont été infectés et récupérés suite à leurs réponses immunitaires. Par exemple, voir l’étude de terrain sur les anticorps pour la Californie réalisée par Bendavid et al, 2020).
Ceci est illustré pour la Californie à la figure 9 et pour le Texas à la figure 10.
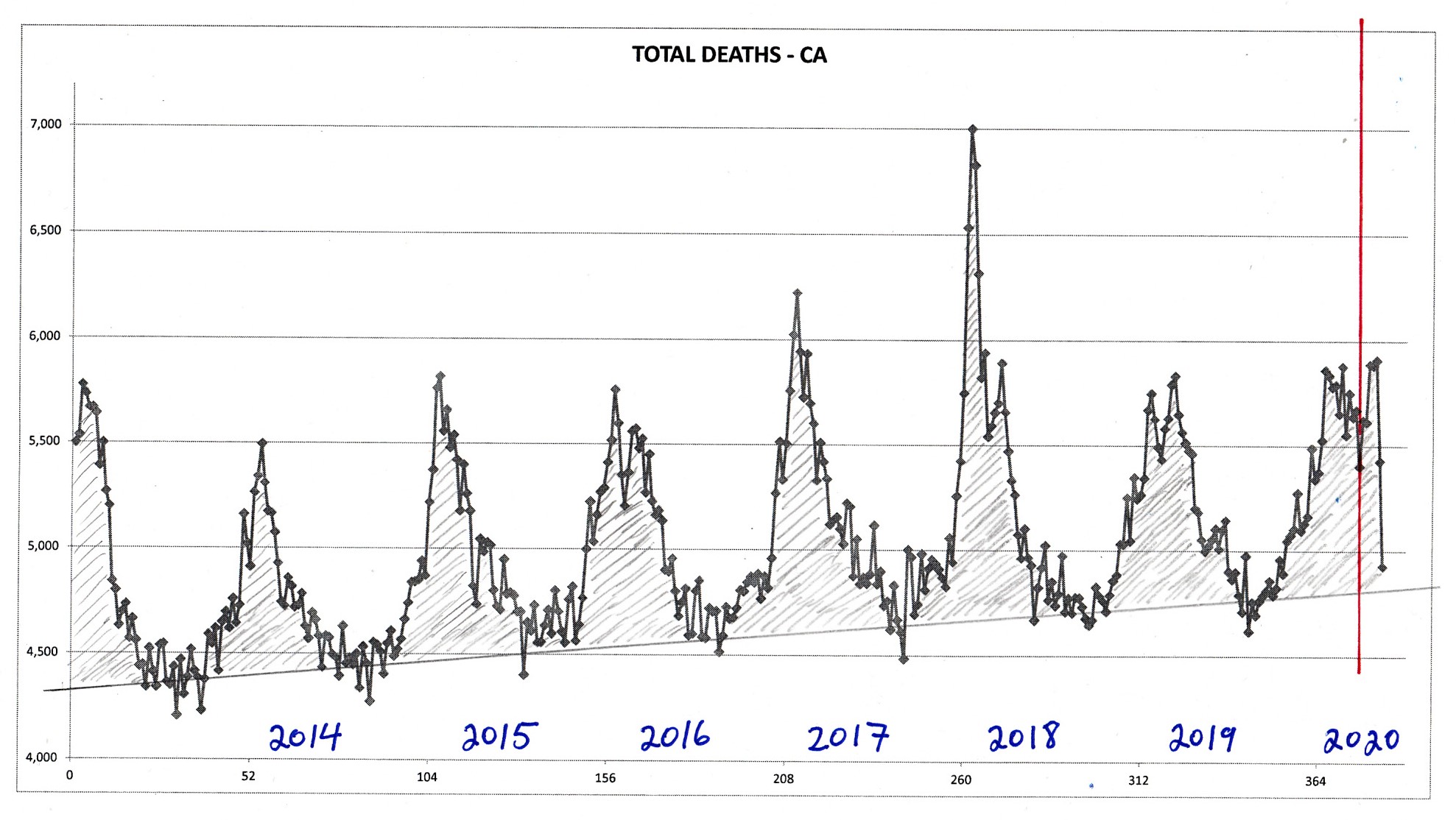
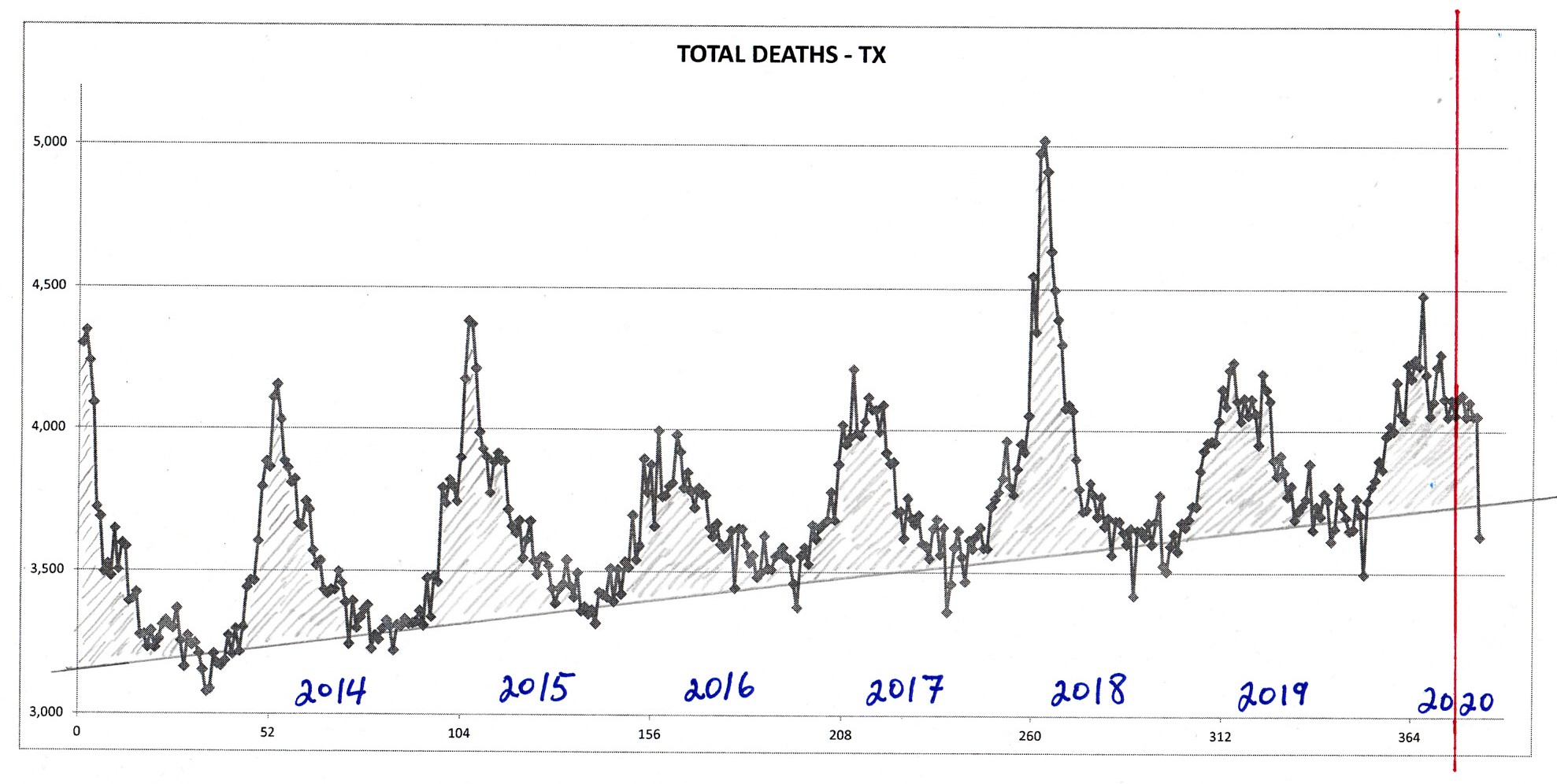
De plus, aucun des sept États qui n’ont pas imposé de confinement (Iowa, Nebraska, Dakota du Nord, Dakota du Sud, Utah, Wyoming et Arkansas) n’a de « pic COVID ».
La présence d’un « pic COVID » est positivement corrélée avec la part des décès attribués selon COVID-19 survenant dans les maisons de retraite et les centres de vie assistée, selon cette carte :
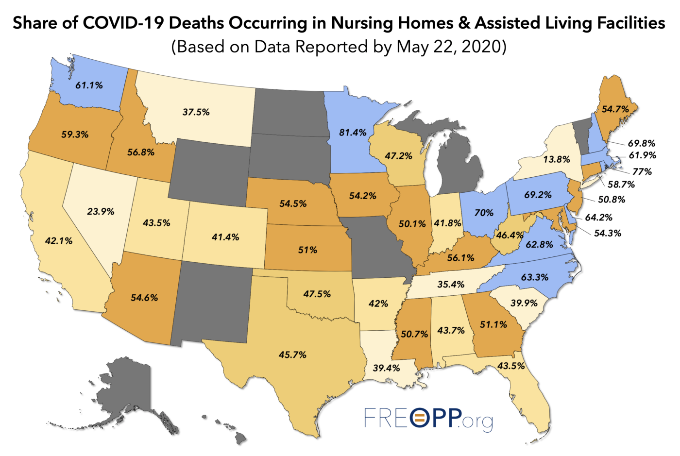
Interprétation du « pic COVID » dans la mortalité toutes causes confondues
Étant donné le caractère unique du « pic COVID » de la mortalité toutes causes confondues :
- Sa netteté, avec une largeur à mi-hauteur maximale de seulement 4 semaines environ ;
- Son retard dans le cycle de la saison infectieuse, qui augmente après la semaine 11 de 2020, ce qui est sans précédent pour toute caractéristique de pic aigu ;
- La synchronisation du début de sa poussée, sur tous les continents, et immédiatement après la déclaration de la pandémie par l’OMS ; et
- Son absence ou sa présence d’un état à l’autre des États-Unis pour la même écologie virale sur le même territoire, est corrélée aux événements dans les maisons de retraite et aux actions du gouvernement plutôt qu’à un quelconque discernement de la souche virale connue.
Compte tenu de l’examen ci-dessus des connaissances sur les maladies respiratoires virales saisonnières :
- Les schémas de mortalité toutes causes confondues, robustes, persistants et réguliers de la charge hivernale, à travers l’ère moderne de l’épidémiologie et entre les nations de deux hémisphères ;
- La nouvelle compréhension (2010) que la transmissivité est contrôlée par l’humidité absolue, et que le vecteur de transmission est constitué de petites particules d’aérosol qui pénètrent profondément dans les poumons ;
- La reconnaissance croissante de la budgétisation de l’énergie métabolique comme paradigme pour comprendre la mort par maladies infectieuses avec des conditions de comorbidité, tout en reconnaissant que le système immunitaire a un contrôle hiérarchique sur la budgétisation de l’énergie métabolique, en second lieu après la connaissance d’un danger externe imminent ; et
- La compréhension croissante du rôle dominant du stress métabolique (y compris la cognition du stress, le stress perçu) dans la diminution de la capacité de réponse du système immunitaire.
Je postule que le « pic COVID » représente un homicide de masse accéléré de personnes immunovulnérables, et de personnes rendues plus immunovulnérables, par des actions gouvernementales et institutionnelles, plutôt qu’une signature épidémiologique d’un nouveau virus, indépendamment du degré de nouveauté du virus du point de vue de la spéciation virale.
Enfin, mon interprétation du « pic COVID » comme étant la signature d’un homicide de masse par la réaction du gouvernement est étayée par plusieurs documents institutionnels, rapports de médias et articles scientifiques, comme les exemples suivants.
Deux articles scientifiques abordent ce sujet :
- Hawryluck et autres (2004), sur le syndrome de stress post-traumatique (SSPT) résultant d’une quarantaine médicale.
- Richardson et al. (2020), sur la preuve statistique que les ventilateurs mécaniques ont tué des patients atteints de COVID-19 critique.
Parmi les articles de presse et les mémos institutionnels, on peut citer
- « Une nouvelle étude révèle que presque tous les patients atteints de coronavirus mis sous respirateur sont morts« , News Break | The Hill 04-23, 23 avril 2020.
« De nouvelles données sur les soins de santé suggèrent que près de la moitié des patients atteints de coronavirus placés sous respirateur meurent, selon le premier rapport de CNN. Les données ont été recueillies à Northwell Health, le plus grand système hospitalier de l’État de New York. Elles ont révélé qu’environ 20% des patients atteints de COVID-19 sont décédés, et que 88 % des patients placés sous respirateur sont morts ». - « La fille blâme le ‘chaos’ de la pandémie de COVID-19 pour le déclin rapide de sa mère« , par Arthur White-Crummey, Regina Leader-Post, 29 mai 2020.
« La mère de Sue Nimegeers n’a jamais eu le COVID-19, mais elle la compte toujours parmi les victimes de la maladie. Elle n’a jamais été testée positive, mais le chaos de la pandémie elle-même autour de nous, nous le pensons, nous l’a prise beaucoup trop tôt », a déclaré Nimegeers au conseil d’administration de l’Autorité sanitaire du Saskatchewan (SHA) vendredi. - « Un rapport « profondément inquiétant » sur les foyers de soins de l’Ontario a été publié« , BBC, 27 mai 2020.
« M. Ford a déclaré qu’une enquête complète a été lancée sur les allégations selon lesquelles les installations sentaient la nourriture pourrie, infestée de cafards et de mouches, et que des personnes âgées étaient laissées pendant des heures criant au secours alors que le personnel ne répondait pas ». - « Rien ne peut justifier cette destruction de vies humaines« ,
Yoram Lass, ancien directeur du ministère de la santé israélien, sur
l’hystérie autour de Covid-19, spiked-online, 22 mai 2020.
« Yoram Lass : C’est la première épidémie de l’histoire qui s’accompagne d’une autre épidémie – le virus des réseaux sociaux. Ces nouveaux médias ont entraîné un lavage de cerveau de populations entières. Ce que vous obtenez, c’est de la peur et de l’anxiété, et une incapacité à regarder les vraies données. Et donc, vous avez tous les ingrédients pour une hystérie monstrueuse. C’est ce qu’on appelle en science un feedback positif ou un effet boule de neige. Le gouvernement a peur de ses électeurs. C’est pourquoi il met en œuvre des mesures draconiennes. Les électeurs regardent les mesures draconiennes et deviennent encore plus hystériques ».
– Cuomo minimise les appels à une enquête fédérale sur les décès dus aux coronavirus dans les maisons de retraite : « Demandez au président Trump« , par Andrew O’Reilly | Fox News, 20 mai 2020.
« Le gouverneur new-yorkais Andrew Cuomo a rejeté mercredi les appels au ministère de la justice pour qu’il ouvre une enquête sur le nombre massif de décès dans les maisons de retraite de l’État lors de la pandémie de coronavirus – affirmant qu’il ne faisait que suivre les directives de l’administration Trump et des Centers for Disease Control and Prevention. Bien qu’aucune enquête officielle n’ait été annoncée, cette spéculation intervient alors que sa directive du 25 mars dernier, qui exigeait que les maisons de retraite accueillent de nouveaux patients infectés par le COVID-19, est passée au crible ». - DATE : 25 mars 2020
A : Administrateurs de maisons de soins infirmiers, directeurs de soins infirmiers et planificateurs de sorties d’hôpital
DE : Département de la santé de l’État de New York
Conseil : sorties d’hôpital et admissions dans les maisons de soins
(Supprimé de : coronavirus.health.ny.gov)
« Pendant cette urgence sanitaire mondiale, toutes les maisons de retraite doivent se conformer à la réception accélérée des résidents qui reviennent des hôpitaux. Les résidents sont jugés aptes à retourner dans un établissement de soins de santé lorsque le médecin de l’hôpital ou son représentant détermine que le résident est médicalement stable pour le retour. […] Aucun résident ne peut se voir refuser sa réadmission uniquement sur la base d’un diagnostic confiné ou suspecté de COVID-19. Il est interdit aux maisons de retraite d’exiger d’un résident hospitalisé qui est déterminé comme étant médicalement stable qu’il subisse un test de COVID-19 avant son admission ou sa réadmission ». - « Les foyers de soins et les centres de vie assistée représentent 42 % des décès par COVID-19 : Une statistique surprenante qui a de profondes implications sur la façon dont nous avons géré la pandémie de coronavirus », par Gregg Girvan, FREOPP, 7 mai 2020.
« Sur la base d’une nouvelle analyse des rapports de décès COVID-19 par État, il est clair que l’aspect le plus sous-estimé de la nouvelle pandémie de coronavirus est son effet sur une population spécifique d’Américains : ceux qui vivent dans des maisons de soins infirmiers et des centres d’assistance ». - « Coupable – de respirer« , par Tony Heller, Tony Heller YouTube Channel, 24 mai 2020.
« Les confinements ont été vendus il y a des mois dans l’idée d' »aplatir la courbe ». Dans la plupart des endroits, il n’y a jamais eu beaucoup de courbe à aplatir, mais les dispositifs de confinement sont toujours en place. Des dizaines de millions de personnes voient aujourd’hui leur vie détruite – pour crime de respiration ». - « Le « massacre »
des résidents des maisons de retraite en Italie : Les patients atteints
de Covid-19 dans l’épicentre du virus en Italie, en Lombardie, ont été
transférés dans des maisons de retraite par une résolution officielle
aux conséquences catastrophiques », par Maria Tavernini et Alessandro Di Rienzo, TRT World, 20 avril 2020.
« Accueillir des patients du Covid-19 dans des maisons de retraite, c’était comme allumer une allumette dans une botte de foin. » - « Mise
à jour Coronavirus : Comment le renforcement des hôpitaux pour le
COVID-19 a contribué à la crise des soins de longue durée au Canada« , par Jessie Willms et Hailey Montgomery, Globe & Mail, 20 mai 2020.
« La plupart des résidents des maisons de retraite et de soins qui ont succombé au COVID-19 au Canada sont morts dans des établissements frappés par le virus et manquant de personnel, les lits d’hôpitaux étant vides ». - « Il n’y a pas de preuve que les confinements ont sauvé des vies. Il est incontestable qu’ils ont causé un grand préjudice« , par Briggs, wmbriggs.com, 14 mai 2020.
« En fin de compte, cela ne se résume pas à des statistiques au niveau du pays ou même de la ville. C’est une question de personnes. Chaque individu attrape le virus ou non, vit ou meurt. Pas à cause de son pays, mais à cause de lui-même, de sa santé, de sa situation. Tout individu peut avoir bénéficié d’une mise en quarantaine et d’une perte d’emploi. Tout comme n’importe quel individu peut avoir connu une mauvaise fin après un confinement ». - « Les hôpitaux sont mieux payés pour inscrire leurs patients sur la liste COVID-19« , par Tom Kertscher, POLITIFACT, 21 avril 2020.
« La norme veut que l’assurance maladie paie à l’hôpital environ trois fois plus pour un patient qui utilise un respirateur que pour un autre. L’assurance-maladie ajoute 20 % à ses paiements réguliers aux hôpitaux pour le traitement des victimes du COVID-19. C’est le résultat d’une loi fédérale de relance ». - « CDC : 80 000 personnes sont mortes de la grippe l’hiver dernier aux États-Unis, le plus grand nombre de décès en 40 ans« , par Associated Press, STAT News, 26 septembre 2018.
« On estime que 80 000 Américains sont morts de la grippe et de ses complications l’hiver dernier – le plus grand nombre de décès dus à cette maladie depuis au moins quatre décennies. Le directeur des Centers for Disease Control and Prevention, le Dr Robert Redfield, a révélé ce total dans une interview accordée mardi soir à The Associated Press ».
Chercheur, Association des libertés civiles de l’Ontario (ocla.ca)
Références scientifiques
- Alimpiev, Egor (2019) « Rethinking the Virus Species Concept« , daté du 15 mars 2019, posté sur stanford.edu
- Baccam, P. et autres (2006) « Kinetics of Influenza A Virus Infection in Humans« , Journal of Virology juillet 2006, 80 (15) 7590-7599 ; DOI : 10.1128/JVI.01623-05
- Bajgar et al. (2015) « Extracellular Adenosine Mediates a Systemic Metabolic Switch during Immune Response« , PLoS Biol 13(4) : e1002135.
- Bendavid et al. (2020) « COVID-19 Antibody Seroprevalence in Santa Clara County, California« , medRxiv 2020.04.14.20062463 ; doi
- Brooke, C. B. et al (2013) « Most Influenza A Virions Fail To Express at least One Essential Viral Protein« , Journal of Virology Feb 2013, 87 (6) 3155-3162 ; DOI : 10.1128/JVI.02284-12
- Dowell, S. F. (2001) « Seasonal variation in host susceptibility and cycles of certain infectious diseases« , Emerg Infect Dis. 2001;7(3):369-374. doi:10.3201/eid0703.010301
- Haas, C.N. et autres (1993) « Risk Assessment of Virus in Drinking Water », Risk Analysis, 13 : 545-552. doi:10.1111/j.1539-6924.1993.tb00013.x
- Harper, G J. (1961) « Airborne micro-organisms : survival tests with four viruses« , The Journal of hygiene, vol. 59,4 : 479-86. doi:10.1017/s0022172400039176
- Hawryluck, L. et autres (2004) « SARS control and psychological effects of quarantine, Toronto, Canada« , Emerging infectious diseases, vol. 10,7 : 1206-12. doi:10.3201/eid1007.030703
- HealthKnowlege-UK (2020) « Charte 1a – Epidémiologie : Théorie des épidémies (chiffres de reproduction effective et de base, seuils épidémiques) et techniques d’analyse des données relatives aux maladies infectieuses (construction et utilisation de courbes épidémiques, chiffres de génération, rapports exceptionnels et identification des groupes importants) », HealthKnowledge.org.uk, consulté le 2020-04-10.
- Hsieh, Y.C. et autres (2006) « Influenza pandemics : past, present and future », J Formos Med Assoc. 105(1):1-6. doi:10.1016/S0929-6646(09)60102-9
- Langmuir, A.D. (1976) « William Farr : Founder of Modern Concepts of Surveillance« , International Journal of Epidemiology, Volume 5, Numéro 1, mars 1976, Pages 13-18
- Locey et Lennon (2016) « Scaling laws predict global microbial diversity« , Proceedings of the National Academy of Sciences, mai 2016, 113 (21) 5970-5975 ; DOI : 10.1073/pnas.1521291113
- Lowen, A. C. et al (2007) « Influenza Virus Transmission Is Dependent on Relative Humidity and Temperature« , PLoS Pathog 3(10) : e151.
- Lui, K.J., Kendal, A.P. (1987) « Impact of influenza epidemics on mortality in the United States from October 1972 to May 1985« , Am J Public Health, 77(6):712?716. doi:10.2105/ajph.77.6.712
- Marti-Soler, H. et al (2014) « Seasonal Variation of Overall and Cardiovascular Mortality : A Study in 19 Countries from Different Geographic Locations« , PLoS ONE, 9(11) : e113500.
- Rancourt, D.G. (2020), « Masks Don’t Work : A review of science relevant to COVID-19 social policy« , Rapport technique, Research Gate, 10 avril 2020, DOI : 10.13140/RG.2.2.14320.40967/1
- Richardson, S. et autres (2020) « Presenting Characteristics, Comorbidities, and Outcomes Among 5700 Patients Hospitalized With COVID-19 in the New York City Area« , JAMA. 323(20):2052-2059. doi:10.1001/jama.2020.6775
- Sapolsky (2005) « The Influence of Social Hierarchy on Primate Health« , Science, 29 avril 2005, vol. 308, pages 648-652. DOI : 10.1126/science.1106477
- Sapolsky (2015), « Stress and the brain : individual variability and the inverted-U« , Nature Neuroscience, octobre 2015, vol. 18, no. 10, pages 1344-1346. doi : 10.1038/nn.4109.
- Shaman, J. et al (2010) « Absolute Humidity and the Seasonal Onset of Influenza in the Continental United States« , PLoS Biol 8(2) : e1000316.
- Simonsen, L. et autres (1997) « The impact of influenza epidemics on mortality : introducing a severity index« , Am J Public Health. 87(12):1944?1950. doi:10.2105/ajph.87.12.1944
- Straub RH. (2017) « Le cerveau et le système immunitaire provoquent une pénurie d’énergie dans les cas d’inflammation chronique et de vieillissement« , Nat Rev Rheumatol. 13(12):743?751. doi:10.1038/nrrheum.2017.172
- Viboud, C. et autres (2010) « Preliminary Estimates of Mortality and Years of Life Lost Associated with the 2009 A/H1N1 Pandemic in the US and Comparison with Past Influenza Seasons« , PLoS currents, vol. 2 RRN1153. 20 mars 2010, doi:10.1371/currents.rrn1153
- Viboud C. et autres (2006) « Transmissibilité et impact de la mortalité de la grippe épidémique et pandémique, avec un accent particulier sur l’épidémie exceptionnellement mortelle de 1951« , Vaccine. 24(44-46):6701?6707. doi:10.1016/j.vaccine.2006.05.067
- Viboud, C. et autres (2005) « Multinational Impact of the 1968 Hong Kong Influenza Pandemic : Evidence for a Smoldering Pandemic« , The Journal of Infectious Diseases, Volume 192, Numéro 2, 15 juillet 2005, Pages 233-248
- Yang, W. et al (2011) « Concentrations et distributions de taille des virus de la grippe A transmis par l’air mesurées à l’intérieur d’un centre de santé, d’une garderie et dans les avions« , Journal of the Royal Society, Interface. 2011 Aug;8(61):1176-1184. DOI : 10.1098/rsif.2010.0686.
- Yezli, S., Otter, J.A. (2011) « Minimum Infective Dose of the Major Human Respiratory and Enteric Viruses Transmitted Through Food and the Environment« , Food Environ Virol 3, 1-30.
- Zwart, M. P. et autres (2009) « An experimental test of the independent action hypothesis in virus-insect pathosystems« , Proc. R. Soc. B. 2762233-2242
Notes
- Voir : « Le système immunitaire : Cellules, tissus, fonction et maladie« , revue médicale par Daniel Murrell, MD le 11 janvier 2018 – Rédigée par Tim Newman, sur medicalnewstoday.com, consulté le 1er juin 2020 "↩"
- « Discours d’ouverture du directeur général de l’OMS lors du point de presse sur COVID-19« – 11 mars 2020 "↩"


Aucun commentaire:
Enregistrer un commentaire